[이선 변호사] GMP란 무엇인가? 2
페이지 정보

본문
안녕하세요.
이선 변호사입니다.
지난 포스팅에 이어,
제약분야의 GMP의 개념에 대해 좀더 구체적으로 설명을 드리려고 합니다.
GMP는 의약품의 품질보증체계 확립 및 기타 오염 등 품질변화를 방지하기 위하여 도입된 일종의 풍샌 관리 기준입니다.
어떤 물리적 시설, 예를 들어 공장이 있다고 가정해 볼께요.
그 공장에서 제품을 생산하는 공정에 대한 기준이라고 생각하시면 이해가 쉬우실 것입니다.
그 공정에 대한 기준, GMP를 인정하면, 의약품에 GMP마크를 받을 수 있는 것이지요.
GMP 기준은 기본적으로 의약품의 품목별로 규정되어 있습니다.
당연하겠지요.
각각의 의약품의 특성이 다르기 때문에 그것을 생산하는 원료를 조달하고, 어떤 온도에서 어떻게 보관하고, 어떻게 조합하여 만드는지 그 기준이 다 다릅니다.
그래서 이러한 기준에 맞는 생산을 유지·관리하고, 이를 검사하고 교정하는 기준이 각각 세부적으로 정해져 있는 것이지요.
이러한 세부적인 규정을 아우르는 일반적인 원칙은,
"의약품 등의 안전에 관한 규칙"이며, 이 규칙의 상위 법령이 약사법이라고 보시면 됩니다.
잠깐만요.
그렇다면, 품목허가를 받지 못한 약은 GMP규정이 없는 걸까요?
그렇지 않습니다.
임상연구를 위한 의약품의 경우에도
의약품 제조 및 품질관리기준에 따라
임상시험용의약품 제조 및 품질관리기준이 있고, 이를 충족하여 약을 생산하여야 합니다.
그리고,
이 "의약품 제조 및 품질관리에 관한 규정"에 따라
식약처(식품의약품안전처)는 내부지침으로 각 의약품의 GMP 평가 가이드라인을 만들어 배포하고
이 가이드라인에 따라, GMP시설을 검사하고 교정 명령을 내리는 등
GMP 시설을 관리하여 합격하는 시설에 한해서 다시 GMP 시설이라는 Certificate을 부여합니다.
그래서 그 Certificate을 보면, 언제 검교정을 했고, 그래서 언제부터 언제까지 한시적으로 GMP시설이라고 인정하는 내용이 나타나있죠.
작년 3월자 기사 중 하나를 예시로 가져와 봤습니다.
https://www.pharmnews.com/news/articleView.html?idxno=220234
이와 같이 식약처가 각 GMP 시설을 각 기준에 맞추어 실사를 하고, 보정명령을 내려 교정하여 시설을
유지할 것인지, GMP 시설이라는 타이틀을 박탈할 것인지 결정하게 됩니다.
예시로,
임상시험의약품의 GMP 가이드라인을 한번 보여드리겠습니다.

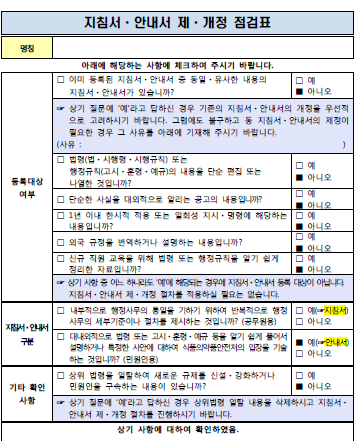

이 가이드라인에는 임상시험용 의약품의 GMP평가를 위한 제출자료도 안내하고, 이 제출자료 중에는
제품품질평가 기준서, 운영실적, 벨이데이션 실시 보고서, 결과 보고서 등을 포함하고 있습니다.
다른 의약품의 GMP 가이드라인의 체계도 이와 유사합니다.
품목별로 그 세부사항이 다른 것이지요.
더 궁금하신 부분이 있으시면
법무법인 (유한) 라움 이선 변호사실로 연락주시기 바랍니다.
관련링크
- 이전글[이선 변호사] M&A 전문가란 누구인가? 24.02.21
- 다음글[이선 변호사] GMP의 개념 24.02.21
댓글목록
등록된 댓글이 없습니다.






